Por Júlio Bernardes– Jornal da USP
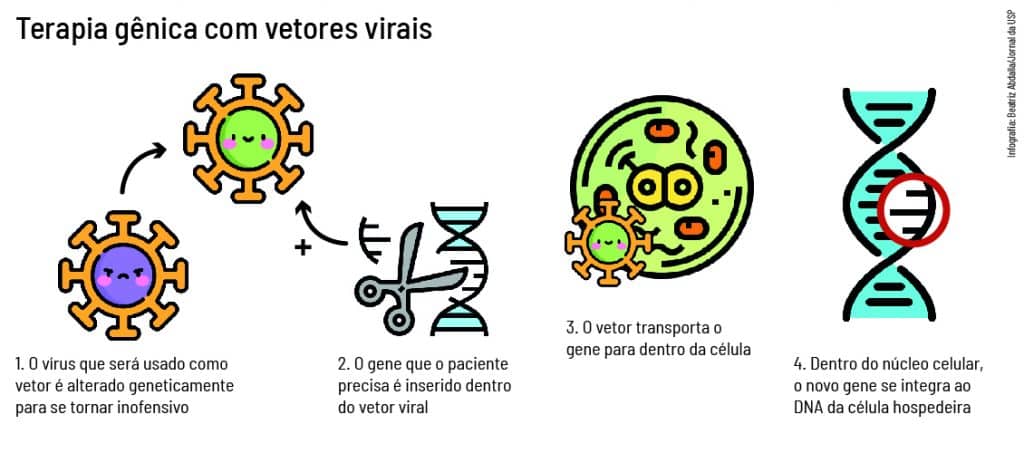
Apesar de ainda soar algo espantoso, utilizar vírus modificados como vetores em terapia genética não chega a ser uma novidade na ciência. Mas as técnicas vêm sendo aprimoradas. Uma nova estratégia nesta linha, aplicada para destruir tumores de pulmão, foi testada com sucesso em pesquisa do Instituto de Ciências Biomédicas (ICB) da USP. Ao contrário do método convencional, onde o chamado vetor de transferência gênica – geralmente um vírus modificado em laboratório – introduz apenas um gene terapêutico na célula doente, a técnica desenvolvida no ICB usa um único vírus para transferir ao mesmo tempo dois genes supressores de tumor. Ao chegarem ao núcleo das células tumorais, esses genes causam a morte celular. Em experimentos com animais, o novo método reduziu os tumores cancerígenos em até 80% e os pesquisadores preparam-se para iniciar os testes em seres humanos. A descoberta é relatada em artigo da revista Gene Therapy, editada pelo grupo Nature.
O que a terapia gênica faz é utilizar esses vírus – neste caso, um adenovírus modificado, que não causa doenças – para levar até o núcleo das células cancerígenas um gene que impeça o crescimento e destrua os tumores. “As células tumorais não querem envelhecer e nem morrer, por isso continuam a se dividir indefinidamente”, conta a professora Eugenia Constanzi Strauss, coordenadora da pesquisa. “Em praticamente todos os tumores cancerígenos, essa divisão é causada por problemas no controle do ciclo de vida das células (proliferação, envelhecimento e morte), motivados por mutações em dois alvos comuns, os genes p53 e CDKN2A.”

Quando o p53 está intacto, ele identifica situações de estresse nas células, como a presença de mutações que podem levar à proliferação exagerada e ao câncer. “Esse gene aciona proteínas que contornam essa situação e, caso elas não funcionem, induz à morte das células”, diz Eugênia. “O CDKN2A é um gene ligado ao envelhecimento das células, porque ele bloqueia definitivamente o processo de divisão”.
Segundo a professora, como o câncer é uma doença que envolve vários genes, faz sentido a ideia de tentar remediar várias mutações de uma só vez. “Assim, a pesquisa desenvolveu um vetor bicistrônico, que recebe esse nome por ser capaz de transferir simultaneamente os p53 e o CDKN2A para as células tumorais”, explica. “O novo vetor, um adenovírus, foi usado em experimentos com células de tumores do pulmão, um tipo de câncer de grande interesse epidemiológico, devido a sua alta frequência na população, independente do sexo.”
Destruindo tumores
Inicialmente, o vetor foi testado in vitro (em experimentos de bancada), em linhagens de células de tumores de pulmão humano cultivadas em laboratório, nas quais o gene pP53 e CDKN2A sofreram mutações. “Os resultados foram excelentes. O vírus com os dois genes é melhor que as versões com apenas um gene”, ressalta Eugênia. “Os genes induzem à morte maciça das células tumorais, e a atuação conjunta do p53 e do CDKN2A estabelece novamente a barreira contra a divisão celular anormal.” Os testes in vivo (com modelos animais) foram feitos em camundongos no quais foram implantadas células tumorais, obtendo-se uma redução de até 80% do tamanho dos tumores em um período de 30 a 45 dias após a introdução do vírus modificado.
“Novos experimentos vão combinar a terapia genética com o uso de medicamentos quimioterápicos, que poderão tornar a quimioterapia mais branda com a redução da dose e, em consequência, dos efeitos adversos”, destaca a professora. “O vetor também vai ser usado em células de tumores do sistema nervoso central, os glioblastomas, um tipo de tumor com poucas opções de tratamento.”
O próximo passo da pesquisa é a produção dos vetores em um laboratório piloto, seguindo as normas da Anvisa, adotadas pela indústria farmacêutica. “Até agora, o que se tem é o protótipo de um produto para terapia gênica. Para que ele chegue aos hospitais, é preciso fazer várias etapas de ensaios pré-clínicos em seres humanos, a primeira delas para verificar a toxicidade”, relata Eugênia. “Esses testes exigem a que os vetores sejam produzidos com qualidade para uso clínico, seguindo um processo conhecido como Boas Práticas de Produção (GMP, na sigla em inglês). Após o sucesso dos protocolos clínicos experimentais,a tecnologia pode ser transferida para as indústrias.”
A professora ressalta que a Anvisa publicou em 20 de fevereiro uma resolução que regulamenta os produtos para terapias avançadas, inclusive a terapia genética. “Em todo o mundo, estima-se que haja 20 produtos de terapia gênica licenciados, número que pode chegar a 300 em dez anos. O custo dos vetores ainda é altíssimo, e com a resolução, as empresas podem licenciar, produzir e vender no Brasil”, afirma. “Esse processo pode levar alguns anos e o trabalho da universidade é desenvolver a tecnologia e realizar estudos de prova de princípio a partir do zero, mapeando toda a rota, do laboratório ao leito do paciente, e também formar recursos humanos que permitam a transferência do conhecimento à indústria, capacitando-a para realizar a produção.”
Mais informações: e-mail [email protected], com a professora Eugênia Constanzi Strauss
***
Capa: Ao contrário da terapia genética convencional, onde em geral um vírus modificado em laboratório introduz apenas um gene terapêutico na célula doente, nova técnica utiliza um único vírus para transferir dois genes supressores de tumor, que ao chegarem ao núcleo das células causam morte celular – Ilustração: Cleber Siquette/Jornal da USP